Bài 1 trang 25 SGK Vật lí 12
Lời giải
Bài Tập và lời giải
I.Trắc nghiệm khách qua
Câu 1: Phân tử chất hữu cơ X có 2 nguyên tố C, H. Tỉ khối hơi của X so với hidro là 22. Công thức phân tử của X là?
A.C4H8 B.C3H8
C.C3H6 D.C6H6
Câu 2: Cho công thức cấu tạo của các chất (I), (II), (III)
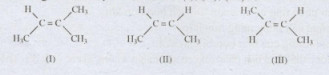
Các chất có cùng công thức phân tử là
A.(II), (III). B.(I), (III)
C.(I),(II) D.(I), (II), (III).
Câu 3: Đốt cháy hoàn toàn m gam một hợp chất hữu cơ X (có chứa 2 nguyên tố C, H) thu được 3,36 lít CO2 (đktc) và 4,5 gam H2O. Giá trị của m là (H = 1, C = 12, O = 16)
A.4,6 gam
B.2,3 gam
C.11,1 gam
D.không thể xác định
Câu 4: Để biết phản ứng: CH4 + Cl2 \(\to\) CH3Cl + HCl (ánh sáng) đã xảy ra hay chưa người ta
A.kiểm tra sản phẩm phản ứng bằng quỳ tím ẩm, quỳ tím hóa đỏ tức phản ứng đã xảy ra.
B.chỉ cần cho thể tích CH4 bằng thể tích Cl2.
C.kiểm tra thể tích hỗn hợp khí, nếu có phản ứng xảy ra thì thể tích hỗn hợp tăng.
D.có thể kiểm tra clo, nếu clo còn tức phản nwgs chưa xảy ra.
Câu 5: Phản ứng: 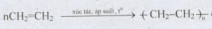 được gọi là phản ứng
được gọi là phản ứng
A.trùng hợp B.cộng
C.hóa hợp D.trùng ngưng
Câu 6: Đốt cháy 2,6 gam một chất hữu cơ X, người ta thu được 8,8 gam CO2 và 1,8 gam H2O. Tỉ khối hơi chất X đối với H2 là 13. Công thức phân tử chất X là (H = 1, C = 12, O = 16)
A.C2H4 B.C2H2
C.CH4 D.C6H6.
Câu 7: Thể tích không khí (O2 chiếm 20% theo thể tích, đktc) cần để đốt cháy 2,6 gam C2H2 là (cho H = 1, C = 12)
A.3,36 lít B.4,48 lít
C.13,44 lít D.28 lít.
Câu 8: Trong những hidrocacbon sau, những chất nào có phản ứng thể với brom?
\(\eqalign{ & C{H_3} - C{H_3},C{H_3} - CH = C{H_2},\cr&C{H_3} - C \equiv CH,{C_6}{H_6}. \cr & A.C{H_3} - C{H_3},C{H_3} - CH = C{H_2} \cr & B.C{H_3} - C \equiv CH,{C_6}{H_6}. \cr & C.C{H_3} - C{H_3},{C_6}{H_6}. \cr & D.C{H_3} - CH = C{H_2},\cr&\;\;\;\;\;C{H_3} - C \equiv CH. \cr} \)
II.Tự luận
Câu 9 : Etilen và axetilen có tính chất hóa học giống nhau và khác nhau ở những điểm nào?
Câu 10 : Tính thể tích khí C2H2 (đktc) tạo ra khi cho 10 gam CaC2 (có 36% tập chất) tác dụng hết với H2O (cho C = 12, Ca = 40).
Câu 11: Một hỗn hợp gồm C2H2 và C2H4 có thể tích 5,6 lít khí (đktc) cho qua dung dịch Br2 (dư), dung dịch này nặng thêm 6,8 gam.
Tính thể tích mỗi khí trong hỗn hợp ban đầu (cho H = 1, C = 12).
I.Trắc nghiệm khách quan
Câu 1: Tính chất hóa học đặc trưng của
A.metan là phản ứng thế và etilen là phản ứng cộng.
B.metan và etilen là phản ứng thế.
C.metan và etilen là phản ứng cộng.
D.metan và etilen là phản ứng cháy.
Câu 2: Metan và etilen có sự khác nhau về tính chất hóa học vì phân tử metan
A.chỉ có liên kết đơn còn với etilen ngoài liên kết đơn còn có liên kết đôi.
B.và etilen chỉ chứa 2 nguyên tố C và H.
C.chỉ có 1 nghuyên tử C còn phân tử etilen có 2 nguyên tử C.
D.chỉ có liên kết đơn còn với etilen chỉ có liên kết đôi.
Câu 3: Có thể dùng dung dịch Ca (OH)2, khí O2 để nhận biết các chất nào trong các chất sau: CH4, CO2, N2, H2 ?
A.CH4, N2, H2.
B. CH4, CO2, N2.
C. CO2, N2, H2.
D. CH4, CO2, H2.
Câu 4: Khi chi khí metan tác dụng với khí clo theo tỉ lệ 1:1 về thể tích, sản phẩm phản ứng là:
A.CCl4. B.CHCl3
C.CH2Cl2 D.CH3Cl.
Câu 5: Số công thức cấu tạo của C2H7N, C3H6 m(mạch hở) lần lượt là:
A.2, 1 B.1, 2
C.3, 1 D.3, 2.
Câu 6: Đốt cháy hoàn toàn 784ml khí ( đktc) một hidrocacbon X thu được 3,08 gam CO2 và 0,63 gam nước. Công thức phân tử của X là:
A.C2H4 B.C2H2
C.CH4 D.C6H6.
Câu 7: Dung dịch brom có thể phản ứng với tất cả các chất trong dãy nào sau đây?
\(\eqalign{ & A.C{H_3} - C{H_3},C{H_3} - CH = C{H_2},C{H_3} - C \equiv CH. \cr & B.C{H_3} - C{H_3},C{H_3} - CH = C{H_2},{C_6}{H_6}. \cr & C.C{H_3} - C{H_3},C{H_3} - C \equiv CH,{C_6}{H_6}. \cr & D.C{H_3} - CH = C{H_2},C{H_3} - C \equiv CH. \cr} \)
Câu 8: Đốt cháy 0,3 lít một chất hữu cơ Y (chỉ chứa 2 nguyên tố C, H) người ta thu được 0,6 lít CO2, 0,9 lít hơi H2O (các thể tích đo ở đktc). Công thức phân tử của Y là:
A.C2H6 B.C3H6
C.C3H4 D.C6H6.
II.Tự luận (6 điểm)
Câu 9 (2 điểm): Viết các công thức cấu tạo có thể có của C3H9N (biết C có hóa trị 4, H có hóa trị 1, N có hóa trị 3).
Câu 10 : Một hỗn hợp gồm metan và axetilen có thể tích 4,48 lít (đktc) sục vào dung dịch br2 dư. Dung dịch nặng thêm 3,9 gam.
Tìm thể tích khí O2 (đktc) cần để đốt cháy hết hỗn hợp trên (H = 1, C = 12).
Câu 11 : Một chất hữu cơ Z (chứa các nguyên tố C, H, Cl) trong đó thành phần % theo khối lượng của Cl là: 70,3%, của H là 5,94%.
Biết 0,1 mol chất này có khối lượng 5,05 gam.
Xác định công thức phân tử, công thức cấu tạo của Z (cho H = 1, C = 12, Cl = 35,5).
I.Trắc nghiệm khách quan
Câu 1: Để phân biệt các khí CH4 và H2 người ta
A.đốt từng khí, khí nào cháy được trong khí Cl2 là CH4.
D.đốt từng khí trong bình đựng O2 sau đó rót dung dịch Ca(OH)2 vào bình rồi lắc nhẹ, bình có kết tủa trắng thì khí ban đầu là CH4.
C.chỉ cần biết khí không tan trong nước là khí CH4.
D.chỉ cần biết chất vô cơ là H2.
Câu 2: Cấu tạo phân tử etilen và axetilen khác nhau do
A.số nguyên tử C trong mỗi phân tử.
B.tính chất của chúng khác nhau.
C.etilen có liên kết đôi còn axetilen có liên kết ba.
D.C trong etilen có hóa trị II, còn C trong axetilen có hóa trị I.
Câu 3: Một hữu chất cơ Z khi đốt phản ứng xảy ra theo phương trình:
aZ + 2O2 \(\to\) CO2 + 2H2O.
Công thức phân tử của Z là (a là số nguyên dương)
A.C2H4 B.C3H6
C.C3H8 D.CH4.
Câu 4: Cho phương trình: C6H6 + Br2 \(\to\) C6H5Br + HBr (Fe)
Trong đó:
A.C6H6 là chất lỏng, Br2 là chất khí.
B.C6H5Br là chất lỏng không màu.
C.HBr là chất khí màu nâu đỏ.
D.phản ứng xảy ra ở nhiệt độ rất thấp.
Câu 5: Một bình kín chứa hỗn hợp khí C2H4 và O2, trong bình có mặt dung dịch Br2. Đốt cháy hỗn hợp bằng tia lửa điện, lắc nhẹ bình người ta thấy
A.màu nâu dung dịch Br2 nhạt một phần chứng tỏ C2H4 còn.
B.khối lượng bình nặng hơn so với trước khi đốt.
C.nhiệt độ trong bình không đổi.
D.khối lượng dung dịch Br2 giảm.
Câu 6: Một hidrocacbon X mạch hở, có một liên kết ba trong phân tử. Khi cho 5,2 gam X tác dụng hết với 400ml dung dịch Br2 1M.
X có công thức cấu tạo thu gọn là (H = 1, C = 12)
\(\eqalign{ & A.C{H_3} - CH = C{H_2} \cr & B.C{H_3} - C \equiv CH \cr & C.HC \equiv CH. \cr & D.C{H_3} - C{H_3}. \cr} \)
Câu 7: Cho quá trình: dầu nặng -> xăng + hỗn hợp khí. Quá trình này có tên gọi là:
A.sự phân hủy
B.quá trình crackinh.
C.quá trình trùng hợp.
D.sự chưng cất dầu mỏ.
Câu 8: Một hỗn hợp gồm etilen và metan khi cho qua dung dịch brom dư thì dung dịch tăng 5,6 gam đồng thời có 5,6 lít chất khí bay ra (đktc).
Thành phần % theo thể tích của etilen ban đầu là (H = 1, C = 20)
A.55,56% B.45,45%
C.33,33% D.44,44%.
II.Tự luận
Câu 9 : Mạch cacbon là gì? Có bao nhiêu loại mạch cacbon?
Mỗi loại mạch cacbon lấy 1 ví dụ.
Câu 10: Butan là một hidrocacbon có tính chất tương tự metan và có công thức phân tử là C4H10.
a)Viết công thức cấu tạo của butan.
b)Viết phương trình phản ứng đốt cháy butan.
c)Viết phương trình phản ứng thế với clo.
Câu 11 ( 2 điểm): Đốt cháy hoàn toàn 3,2 gam chất hữu cơ A sản phẩm CO2, và hơi H2O, tạo ra cho qua bình (1) đựng H2SO4 đặc, rồi qua bình (2) đựng dung dịch Ca(OH)2 (dư).
Độ tăng khối lượng (1) là 7,2 gam, bình (2) thu được 20 gam kết tủa.
a)Xác định thành phần % theo khối lượng các nguyên tố trong A.
b) Lập công thức phân tử chất A, biết tỉ khối hơi của A so với không khí là 0,5517. (Cho H = 1, C = 12, O = 16, Ca = 40, Mkk = 29)
I.Trắc nghiệm khách quan
Câu 1: Có thể phân biệt được 2 lít khí C2H4 và SO2 mà chỉ dùng dung dịch
A.Ca(OH)2 B.NaOH
C.NaCl D.Na2CO3.
Câu 2: Cho phản ứng 2CH4 \(\to\) C2H2 + 3H2 (15000C)
Để biết phản ứng đã xảy ra người ta
A.cho hỗn hợp sau phản ứng sục vào dung dịch brom, dung dịch brom mất màu.
B.đốt hỗn hợp sau phản nwgs, sẽ có phản ứng cháy và tỏa nhiều nhiệt.
C.quan sát thấy có hiện tượng sủi bọt do có khí H2 thoát ra.
D.so sánh thể tích hỗn hợp khí trước và sau khi đốt sẽ có sự giảm thể tích.
Câu 3: Số công thức cấu tạo có thể có của phân tử C3H8O là:
A.1 B.3
C.4 D.2
Câu 4: Một dãy các hợp chất có công thức cấu tạo viết gọn:
\(CH \equiv CH,CH \equiv C - C{H_3},\)\(\,CH \equiv C - C{H_2} - C{H_3},...\)
Một hidrocacbon mạch hở, phân tử có cấu tạo tương tự và có n nguyên tử cacbon sẽ có công thức phân tử là:
A.CnH2n+2 B.CnH2n
C.CnH2n-2 D.CnH2n-6.
Câu 5: Hợp chất hữu cơ X chứa các nguyên tố C, H, O trong đó thành phần phần trăm theo khối lượng C là 52,17% và hidro là 13,04%.
Biết khối lượng mol của X là 46 gam. Công thức phân tử của X là (H = 1, C = 12, O = 16)
A.C2H6O B.CH4O
C.C3H8O D.C2H6O2.
Câu 6: Khí C2H2 có lẫn khí CO2, SO2 và hơi H2O. Để thu được C2H2 tinh khiết có thể cho hỗn hợp qua
A.dung dịch KOH (dư), sau đó qua H2SO4 đặc.
B.dung dịch KOH (dư).
C.H2SO4 đặc.
D.H2SO4 đặc, sau đó qua dung dịch KOH (dư).
Câu 7: Đốt cháy hết hỗn hợp gồm metan và axetilen có thể tích 5,6 lít (đktc), cho sản phẩm qua một lượng dư dung dịch Ca(OH)2 thu được 40 gam CaCO3.
Thành phần % theo thể tích của axetilen trong hỗn hợp ban đâu là:
A.60% B.50%
C.40% D.30%
Câu 8: Từ CaC2, nước, người ta có thể điều chế trực tiếp chất nào trong các chất sau?
A.Etan (C2H6)
B.Etilen (C2H4)
C.Axetilen (C2H4)
D.Metan (CH4)
II.Tự luận
Câu 9 : Viết các phương trình phản ứng:
a)Chứng tỏ benzen vừa có khả năng tham gia phản ứng thế, vừa có khả năng tham gia phản ứng cộng (ghi rõ điều kiện).
b)Đốt cháy hợp chất CnH2n+2. Nhận xét về tỉ lệ số mol giữa H2O và CO2 tạo ra.
Câu 10 : Tính thể tích etilen (đktc) cần dùng để điều chế 1kg polietilen.
Biết hiệu suất phản ứng 80% (cho H = 1, C = 12).
Câu 11 : Khi cho metan tác dụng với clo có chiếu sáng người ta thu được nhiều sản phẩm trong đó có chất X, với thành phần % khối lượng cacbon là 14,12%.
Xác định công thức phân tử của A (cho C = 12, H = 1, Cl =35,5).
