Số oxi hóa của Mn là: x = (-2).4 + 1 = +7
=> Chọn D
Câu 15.2.
Những nguyên tố có cùng hoá trị trong các hợp chất với hiđro là
A. N, P, S. B. P, As, Sb.
C. S, Te, Cl. D. F, Cl, P.
Ta có CTCT của các hợp chất với H là:
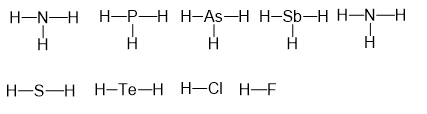
=> P, As, Sb có cùng hóa trị trong hợp chất với H
=> Chọn B
Câu 15.3.
Điện hoá trị của các nguyên tố nhóm VIA, VIIA trong các hợp chất với các nguyên tố nhóm IA lần lượt bằng
A. 2,3. B. 2, 1
C.1,2. D. 1,3.
Công thức của nguyên tố nhóm VIA (A), VIIA (B) với nguyên tố nhóm IA (R) là: R2A, RB
Nguyên tố nhóm IA có điện hóa trị bằng 1+ nên điện hóa trị của nguyên tố nhóm VIA là 2-, điện hóa trị nguyên tố nhóm VIIA là 1-
=> Chọn B
Câu 15.4.
Cộng hoá trị của N là 3, để đạt được cấu hình của khí hiếm thì N phải có
A. 3 liên kết ion.
B. 5 liên kết cộng hoá trị.
C.3 liên kết cộng hoá trị.
D. 5 liên kết ion.
Cộng hóa trị của nguyên tố bằng số liên kết của nguyên tố đó trong hợp chất cộng hóa trị.
N có cấu hình e: 1s22s22p3 thiếu 3e để đạt cấu hình e khí hiếm => cần 3 liên kết => cộng hóa trị 3
=> Chọn C
Câu 15.5.
Nguyên tử A có Z = 15. Trong hợp chất với hiđro, nguyên tử này có khả năng tạo số liên kết cộng hoá trị là
A. 2 liên kết. B. 3 liên kết.
C. 1 liên kết. D. 5 liên kết.
Cộng hóa trị của nguyên tố bằng số liên kết của nguyên tố đó trong hợp chất cộng hóa trị.
Z = 15: 1s22s22p63s23p3 thiếu 3e để đạt cấu hình e khí hiếm => cần 3 liên kết trong hợp chất với H
=> Chọn B