1. Khi đốt cháy A ta thu được CO2 và H2O; vậy A phải chứa C và H.
Khối lượng C trong 1,792 lít CO2 là : \(\dfrac{{12.1,792}}{{22,4}}\) = 0,96 (g).
Khối lượng H trong 1,44 g H2O : \(\dfrac{{2.1,44}}{{18}}\) = 0,16 (g).
Đó cũng là khối lượng C và H trong 3,96 g A.
Theo đầu bài A phải chứa Cl. Khối lượng Cl trong 7,175 g AgCl :
\(\dfrac{{35,5.7,175}}{{143,5}} = 1,775(g)\)
Đó cũng là khối lượng Cl trong 2,475 g A.
Vậy, khối lượng Cl trong 3,96 g A : \(\dfrac{{1,775.3,96}}{{2,475}}\) = 2,840 (g).
Khối lượng C, H và Cl đúng bằng khối lượng chất A (3,96 g).
Vậy, chất A có dạng CxHyClz.
x : y : z = \(\dfrac{{0,96}}{{12}}:\dfrac{{0,16}}{1}:\dfrac{{2,84}}{{35,5}}\) = 0,08 : 0,16 : 0,08 = 1 : 2 : 1
CTĐGN của A là CH2Cl.
2. MA = 3,3.30 = 99 (g/mol)
\( \Rightarrow {(C{H_2}Cl)_n}\) = 99 \( \Rightarrow \) 49,5n = 99 \( \Rightarrow \) n = 2
CTPT của A là C2H4Cl2.
3. Các CTCT
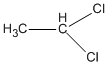 1,1-đicloetan
1,1-đicloetan
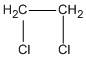 1,2-đicloetan (etylen clorua)
1,2-đicloetan (etylen clorua)