Bước 1:
\({H_2}\mathop S\limits^{ - 2} + K\mathop {Mn}\limits^{ + 7} {O_4} + {H_2}S{O_{4(l)}} \to {H_2}O + \mathop S\limits^0 + \mathop {Mn}\limits^{ + 2} S{O_4} + {K_2}S{O_4}\)
Bước 2:
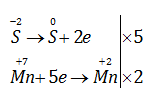
Bước 3:
\(5{H_2}S + 2KMn{O_4} + 3{H_2}S{O_{4(l)}} \to 8{H_2}O + 5S + 2MnS{O_4} + {K_2}S{O_4}\)
=> Chọn B
Câu 17.7.
A. 7 B. 5
C. 4 D. 6
\(\mathop {Zn}\limits^0 \), \(\mathop {Fe}\limits^0 \), \(B{r^ - }\) : chỉ có tính khử
\(\mathop {Fe}\limits^{ + 2} \mathop O\limits^{ - 2} \), \(\mathop S\limits^0 \), \(\mathop S\limits^{ + 4} \mathop {{O_2}}\limits^{ - 2} \),\(\mathop H\limits^{ + 1} \mathop {Br}\limits^{ - 1} \),\(\mathop {{N_2}}\limits^0 \): có cả tính khử và oxi hóa
\(\mathop {Zn}\limits^{ + 2} \mathop O\limits^{ - 2} \),\(\mathop S\limits^{ + 6} \mathop {{O_3}}\limits^{ - 2} \),\(C{u^{2 + }}\): chỉ có tính oxi hóa
=> Chọn B
Câu 17.8.
Cho các phản ứng sau :
\(\begin{array}{l}\left( a \right)\,4HCl + Pb{O_2} \to PbC{l_2} + C{l_2} + 2{H_2}O\\\left( b \right)\,HCl + N{H_4}HC{O_3} \to N{H_4}Cl + C{O_2} + {H_2}O\\\left( c \right)\,2HCl + 2HN{O_3} \to 2N{O_2} + C{l_2} + 2{H_2}O\\\left( d \right)\,2HCl + Zn \to ZnC{l_2} + {H_2}\end{array}\)
Câu 17.9.
A. chất xúc tác.
B. Chất oxi hóa
C. môi trường.
D. chất khử
\(3Cu + 4{H_2}S{O_4} + 2Na\mathop N\limits^{ + 5} {O_3}\xrightarrow{{}}3CuS{O_4} + N{a_2}S{O_4} + 2\mathop N\limits^{ + 2} O + 4{H_2}O\)
Số oxi hóa của N giảm => NaNO3 là chất oxi hóa
=> Chọn B
Câu 17.10.
Cho các phản ứng :
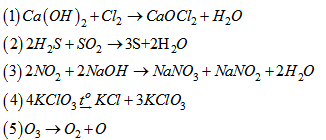
Phản ứng oxi hoá - khử là
A. 1, 2, 3,4,5.
B. 1,2,3.
C. 1,2, 3,4.
D. 1,4.
\(Ca{\left( {OH} \right)_2} + \mathop {C{l_2}}\limits^0 \xrightarrow{{}}Ca\mathop {C{l_2}}\limits^{ - 1} + Ca{(\mathop {Cl}\limits^{ + 1} O)_2} + {H_2}O\)
\(2{H_2}\mathop S\limits^{ - 2} + \mathop S\limits^{ + 4} {O_2}\xrightarrow{{}}3\mathop S\limits^0 + 2{H_2}O\)
\(2\mathop N\limits^{ + 4} {O_2} + 2NaOH\xrightarrow{{}}Na\mathop N\limits^{ + 5} {O_3} + Na\mathop N\limits^{ + 3} {O_2} + {H_2}O\)
\(4K\mathop {Cl}\limits^{ + 5} {O_3}\xrightarrow{{{t^o}}}K\mathop {Cl}\limits^{ - 1} + 3K\mathop {Cl}\limits^{ + 7} {O_4}\)
\(\mathop {{O_3}}\limits^0 \xrightarrow{{}}\mathop {{O_2}}\limits^0 + \mathop O\limits^0 \)
=> (1), (2), (3), (4) là phản ứng oxi hóa-khử
=> Chọn C