Câu 1. Chọn C.
Kim loại kiềm thổ có tính khử yếu hơn kim loại kiềm cùng chu kỳ.
Kim loại kiềm thuộc nhóm IA, kim loại kiềm thổ thuộc nhóm IIA.
Khối lượng riêng của kim loại kiềm thổ đều nhỏ hơn Al (trừ Ba).
Các kim loại kiềm thổ đều mềm nhưng vẫn có độ cứng cao hơn kim loại kiềm.
Câu 2. Chọn B
\(M + 2HCl \to MC{l_2} + {H_2}\)
Ở nhiệt độ thường:
\({O_2}\) không phản ứng với Be, phản ứng chậm với các kim loại còn lại.
\({H_2}O\) không phản ứng với Be, phản ứng chậm với Mg.
Ca, Ba, Sr phản ứng với \({H_2}O\) trong dung dịch \(CuS{O_4}.\)
Câu 3. Chọn A.
Nước cứng dễ tạo kết tủa khi đun nóng hoặc khi kết hợp với các chất khác làm gây cặn bám ở đáy dụng cụ đun nấu gây tốn nhiên liệu, bám vào thành ống dẫn, phản ứng với các chất trong thực phẩm,
Câu 4. Chọn C
X tan một phần \( \to \) X dư, X là Mg.
\(4Mg + 10HN{O_3} \to Mg{(N{O_3})_2}\)\(\, + N{H_4}N{O_3} + 3{H_2}O\)
Fe là kim loại hoạt động trung bình không sinh ra \(N{H_4}N{O_3}.\)
Câu 5. Chọn B
\(CO_3^{2 - } + C{a^{2 + }};M{g^{2 + }} \to CaC{O_3};MgC{O_3}\)
\(Ca{(OH)_2}\) chỉ làm mềm nước cứng tạm thời
Dùng HCl: chỉ có ion \(HCO_3^ - \) phản ứng \( \to \) không làm thay đổi tính cứng.
\(C{a_3}(P{O_4}){ _2}\) không tan, không phản ứng.
Câu 6. Chọn C.
Nước tự nhiên thường chứa \(Ca{(HC{O_3})_2}\) hay còn gọi là nước có tính cứng tạm thời, muốn phân hủy chậm trong tự nhiên sinh ra kết tủa \(CaC{O_3}\) là thành phần chính của thạch nhũ.
Câu 7. Chọn B.
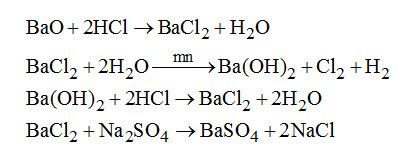
Câu 8. Chọn D.
Các ion không cùng tồn tại nếu kết hợp thành các chất không tan.
Các chất không tan: \(CaC{O_3},BaS{O_4},BaC{O_3}.\)
Câu 9. Chọn A.
Chia 2 trường hợp:
+ \(Ca{(OH)_2}\) dư: \({n_{C{O_2}}} = {n_{CaC{O_3}}} = 0,025\,mol\)
+ \(C{O_2}\) dư so với \(Ca{(OH)_2}\) hòa tan bớt kết tủa còn 0,025 mol.
\( \Rightarrow C{O_2}\) tạo 2 muối \(CaC{O_3}\) và \(Ca{(HC{O_3})_2}\)
\({n_{C{O_2}}} = {n_{CaC{O_3}}} + 2.{n_{Ca{{(HC{O_3})}_2}}} \)\(\,= 0,025 + 2.(0,2 - 0,025) = 0,375\,mol.\)
Câu 10. Chọn C.
\(\begin{array}{l}\overline M + 2HCl \to {H_2} + \overline M C{l_2}\\0,3\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,3\,\,\,\,mol\\\overline M = 29 \to Mg,Ca\end{array}\)