Giải thích ý nghĩa nhan đề bài thơ Tiếng hát con tàu, bình giảng khổ thơ đề từ
Lời giải
Bài Tập và lời giải
Câu 1. Nhận xét nào dưới đây là không đúng. “Trong nhóm halogen, đi từ flo đến iot ta thấy không được”.
A.trạng thái tập hợp: từ thể khí chuyển sang thể lỏng và rắn.
B.màu sắc: đậm dần.
C.nhiệt độ nóng chảy và nhiệt độ sôi: giảm dần.
D.độ âm điện: giảm dần.
Câu 2. Khí hidro clorua là chất khí tan rất nhiều trong nước tạo thành dung dịch axit clohiđric. Trong thí nghiệm thử tính tan của khí hiđrô clorua trong nước, có hiện tượng nước phun mạnh vào bình như hình vẽ mô tả dưới đây. Nguyên nhân dưới đây gây ra hiện tượng đó là
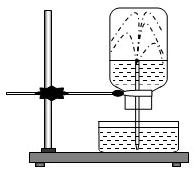
A. do khí hiđro clorua tác dụng với nước hút nước vào bình.
B. do khí hiđro clorua tan mạnh làm giảm áp suất trong bình.
C do trong bình chứa khí hiđro clorua ban đầu không có nước.
D. tất cả các nguyên nhân trên đều đúng.
Câu 3. Chỉ ra đâu không phải là đặc điểm chung của tất cả các halogen?
A. Nguyên tử halogen dễ thu thêm 1 electron.
B. Các nguyên tố halogen đều có khả năng thể hiện các số oxi hóa -1, +1, +3, +5, +7.
C. Halogen là những phi kim điển hình.
D. Liên kết trong phân tử halogen X2 không bền lắm, chúng dễ bị tách thành 2 nguyên tử halogen X.
Câu 4. Các nhà máy xử lý nước cấp luôn mong muốn cung cấp một nguồn nước an toàn và không chứa vi trùng, vi khuẩn gây bệnh. Thêm clo là một trong những phương pháp hiệu quả nhất để khử trùng nguồn nước cấp và đảm bảo chúng không xuất hiện trong quá trình phân phối nước qua đường ống tới người tiêu dùng. Clo được chọn làm chất xử lí nước cấp là do
A.clo tác dụng với nước tạo ra HclO, chất này có tính oxi hóa rất mạnh.
B.clo có tính oxi hóa rất mạnh.
C.clo độc nên có tính sát trùng.
D.Cả B và C.
Câu 5. Hòa tan 28,4g một hỗn hợp 2 muối cacbonat của hai kim kim loại hóa trị II bằng dung dịch HCl dư, thu được 10 lít khi ở \(54,6^\circ C\) và 0,8064 atm và một dung dịch X. Cô cạn dung dịch X thu được m gam muối. Giá trị của m là.
A.30,7 gam. B.31,7 gam.
C.60 gam. D.62,4 gam.
Câu 6. Phản ứng dùng để điều chế clo trong phòng thí nghiệm là
\(\eqalign{ & A.6HCl + KCl{O_3} \to KCl + 3C{l_2} + 3{H_2}O. \cr & B.NaCl\buildrel {dp{\rm{dd}}} \over \longrightarrow Na + {1 \over 2}C{l_2} \uparrow . \cr & C.4HCl + Mn{O_2}\buildrel {t^\circ } \over \longrightarrow C{l_2} \uparrow + MnC{l_2} + 2{H_2}O. \cr & D.2NaCl + 2{H_2}O\mathrel{\mathop{\kern0pt\longrightarrow}\limits_{cmn}^{dp{\rm{dd}}}} C{l_2} \uparrow + {H_2} + 2NaOH. \cr} \)
Câu 7. Trong dãy axit HCl, HI, HF, HBr axit mạnh nhất là
A.HI. B.HCl.
C.HBr. D.HF.
Câu 8. Cho 15,8g KmnO4 tác dụng hoàn toàn với dung dịch HCl đặc, dư thu được V lít khí (đktc). Giá trị của V là
A.5,6 lít. B.4,48 lít.
C.3,36 lít. D. 6,72 lít.
Câu 9. Chỉ dùng duy nhất một loại thuốc thử là AgNO3 có thể nhận ra tối đa bao nhiêu chất trong các dung dịch sau: NaF, NaCl, NaBr, NaI?
A.1 B.2.
C.3. D.4.
Câu 10. Sherlock Homes là một nhà thám tử tư ở Luân Đôn nổi tiếng nhờ sự thông minh, khả năng suy diễn loogic và quan sát tinh tường trong khi phá những vụ án mà cảnh sát phải bó tay. Ông đã phát hiện ra cách lấy dâu vân tay của tội phạm lưu trên đồ vật ở hiện trường chỉ sau ít phút thí nghiệm. Bằng cách đem đồ vật có vân tay đặt đối diện với miệng ống nghiệm chứa chất X, dùng đèn cồn đun nóng ở phần đáy ống nghiệm đến khi xuất hiện luồng khí màu tím bốc ra, dấu vân tay sẽ hiện ra một cách hết sức rõ ràng đến từng đường nét. X là chất nào trong số các chất sau?
A.Clo. B.Flo.
D.Brom. D.Iot.
Câu 11. Sục 0,2016 lít khí clo (đktc) vào 150ml dung dịch NaI 2M ( dung dịch X ). Sau đó, đun sôi đuổi hết iot, thêm nước vào dung dịch cho đủ 200 ml ( dung dịch Y). Nồng độ ml mỗi muối trong dung dịch Y là
A.NaCl 0,09 M.
B.NaCl 0,09 M; NaI 1,41 M.
C.NaI 0,09 M; NaCl 1,41 M.
D.NaCl 0,5M.
Câu 12. Cho 200 ml dung dịch A chưa s hỗn hợp 2 axit HCl 0,4 M và HNO3 0,6M. Để làm kết tủa hết ion Cl- trong A cần cho vào bao nhiêu ml dung dịch AgNO3 0,5M?
A.200ml. B.300 ml.
C. 160 ml. D.100 ml.
Câu 13. Cho hỗn hợp muối ăn có lẫn MgCl2 và NaBr. Để tinh chế NaCl, các bước tiến hành có thể là
A. Hòa tan hỗn hợp vào dung dịch Na2CO3. Cho clo vào dung dịch còn lại. Cô cạn dung dịch.
B. Cho NaOH vào dung dịch có hoonc hợp 2 chất. Cho clo vào dung dịch còn lại. Cô cạn dung dịch.
C. Cho clo vào dung dịch có hỗn hợp 2 chất. Cô cạn dung dịch. Hòa tan chất kết tinh vào dung dịch Na2CO3. Cô cạn dung dịch.
D. Tất cả các đáp án trên đều đúng.
Câu 14. Người ta có thể dùng nhóm hóa chất nào sau đây để khắc chữ khắc hình trên thủy tinh?
A.NaFrắn, H2SO4 đặc.
B.NaCl rắn, H2SO4 đặc.
C.NaBr đặc, H2SO4 đặc.
D.NaBr rắn, H2SO4 đặc.
Câu 15. Cho các phương trình sau đây:
\(\eqalign{ & C{l_2} + X \to Y{\rm{ Z + C}}{{\rm{l}}_2} \to T \cr & Y + Fe \to Z + {H_2}{\rm{ T + NaOH}} \to Fe{\left( {OH} \right)_3} + NaCl \cr} \)
Các chất được kí hiệu là X, Y, Z, T có thể là
|
Đáp án |
X |
Y |
Z |
T |
|
A. |
H2 |
HCl |
FeCl2 |
Cl2 |
|
B. |
H2O |
HClO |
FeCl2 |
FeCl3 |
|
C. |
H2 |
HCl |
FeCl2 |
FeCl3 |
|
D. |
Tất cả đều sai |
|||
Câu 16. Trong đời sống hằng ngày chúng ta thường dùng các chất tẩy trắng như Javen, clorua vôi. Thực tế, chất nào được dùng phổ biến hơn? Vì sao?
A.Nước Javen vì nước Javen dễ tạo chất hơn.
B.Clorua vôi vì clorua vôi có hàm lượng hippoclorit cao.
C.Nước Javen, vì nước Javen có hàm lượng hippoclorit cao, rẻ hơn và dễ bảo quản, vận chuyển hơn.
D.Clorua vôi vì clorua vôi dễ chế tạo hơn.
Câu 17. Trong cỡ thể con người tồn tại một lượng iot tập trung ở tuyến giáp trạng. Ở người trưởng thành lượng iot này khoảng 20 – 50mg. Hàng ngày ta phải bổ sung iot cần thiết cho cơ thể bằng cách ăn muối iot. Nếu lượng iot không cung cấp đủ thì sẽ dẫn đến tuyến giáp trạng sưng to thành bướu cổ, nặng hơn là đần độn, vô sinh và các chứng bệnh khác. Thành phần chính của muối iot là
A.KI và KIO3. B.I2 và KIO3.
C.KI và I2. D.KIO và I3.
Câu 18. Cho m gam KMnO4 tác dụng dung dịch HCl để điều chế đủ khí clo tác với sắt, tạo nên 16.25 gam sắt FeCl3. Giá trị của m là
A.94,8 gam. B.9,48 gam.
C.948 gam. D.0,948 gam.
Câu 19. Nguyên tố halogen có thể đẩy O2 ra khỏi nước là
A. I2. B.Cl2.
D.Br2. D.F2.
Câu 20. Hoàn thành phương trình phản ứng hóa học sau:
\({H_2}S{O_3} + B{r_2} + {H_2}O \to {H_2}S{O_4} + ...\)
Trong dấu ... là
A.HBrO. B.HBrO3.
C.HBrO4. D.HBr.
Câu 21. Cho hình vẽ mô tả sự điều chế Clo trong phòng thí nghiệm như sau:
Phát biểu nào sau đây không đúng?
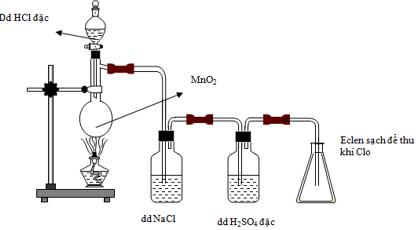
A.Dung dịch H2SO4 đặc có vai trò hút nước, có thể thay H2SO4 bằng CaO.
B.Khí clo thu được trong bình erlen là khí clo khô.
C.Có thể thay MnO2 bằng KMnO4 hoặc KClO3.
D.Không thể thay dung dịch NaCl bằng dung dịch HCl.
Câu 22. Nguyên liệu dùng điều chế nước Javen, clorua vôi, KClO3 có đặc điểm chung là
A.khí clo và axit.
B.khí clo và hiđroxit.
C.khí clo và kim loại.
D. khí clo và muối.
Câu 23. CFC là nguyên nhân chính của
A. hiện tượng mưa axit.
B. sự suy giảm tầng ozon.
C.sự ô nhiễm nguồn nước ngầm.
D.hiện tượng động đất.
Câu 24. Cho hỗn hợp A gồm KBr và KI, hòa tan hoàn toàn A vào nước rồi cho dung dịch brom dư vào dung dịch trên. Đun sôi, cô cạn dung dịch sau phản ứng thì thấy khối lượng sản phẩm B nhỏ hơn khối lượng của A là m gam. Hòa tan sản phẩm B vào nước rồi cho Clo lội qua cho đến dư. Sau phản ứng, cô cạn dung dịch thì thấy khối lượng sản phẩm C nhỏ hơn khối lượng sản phẩm B là m gam. Thành phần % về khối lượng KBr trong hỗn hợp A là
A. 38,7%. B. 56,8%.
D. 3,87%. D. 4,9%.
Câu 25. Phát biểu nào sau đây đúng khi nói về tính chất hóa học của clo trong phương trình phản ứng với nước?
A.Clo thể hiện tính oxi hóa.
B.Clo thể hiện tính khử.
C.Clo vừa thể hiện tính oxi hóa, vừa thể hiện tính oxi hóa.
D.Cả A, B,C đều sai.
Câu 26. Dãy axit nào sau đây được xếp theo thứ tự tính axit tăng dần?
A.HF, HCl, HBr, HI.
B.HI, HBr, HCl, HF.
C.HCl, HF, HI, HBr.
D.HCl, HBr, HI, HF.
Câu 27. Cho lượng dư dung dịch AgNO3 tác dụng với 100ml dung dịch hỗn hợp NaF 0,05M, NaCl 0,1M. Khối lượng kết tủa tạo thành là bao nhiêu?
A.1435 gam. B.1,435 gam.
C.14,35 gam. D.143,5 gam.
Câu 28. Trong phương trình phản ứng sau đây
\(KMn{O_4} + HCl \to KCl + MnC{l_2} + C{l_2} + {H_2}O\)
Hệ số tối giản của các chất trong phương trình hóa học lần lượt là
A. 2, 12, 2, 3, 5, 8.
B. 2, 16, 2, 2, 5, 8.
C. 2, 14, 2, 2, 5, 8.
D. 2, 2, 16, 10, 10.
Câu 29. Những tính chất sau, tính chất nào không phải tính chất của khí hiđroclorua?
A. Tan nhiều trong nước.
B. Tác dụng với khí NH3.
C. Tác dụng với CaCO3 giải phóng khí CO2.
D. Làm đổi màu giấy quỳ tím ẩm.
Câu 30. Trong các dãy sau đây dãy nào tác dụng với dung dịch HCl?
A. AgNO3, MgCO3, BaSO4, MnO2.
B. Fe, CuO, Ba(OH)2, MnO2.
C.Fe2O3, MnO2, Cu, Al.
D. CaCO3, H2SO4, Mg(OH)2, MnO2.
Câu 1. Cho 3,68 gam hỗn hợp CaCO3 và CaO phản ứng vừa đủ với 0,5 lít dung dịch HCl thu được 0,448 lít khí (đktc). Thành phần phần trăm khối lượng của CaCO3 và CaO trong hỗn hợp ban đầu là
A.45,7% và 54,3%.
B.54,3% và 45,7%.
C.57,3% và 42,7%.
D.50,3% và 49,7%.
Câu 2. Hòa tan hoàn toàn 11,9 gam hỗn hợp X gồm Al và Zn bằng dung dịch HCl dư thu được 8,96 lít khí H2 ( đktc ). Thể tích O2 ( đktc ) cần dùng để phản ứng hoàn toàn hỗn hợp X trên là
A.39,2 lít. B.33,6 lít.
C.3,36 lít. D.4,48 lít.
Câu 3. Kem đánh răng chứa một lượng muối flo ( như CaF2, SnF2 ) có tác dụng bảo vệ lớp men răng vì nó thay thế một phần hợp chất có trong men răng là Ca5(PO4)3OH thành Ca5(PO4)3F. Điều này có ý nghĩa quan trọng trong bảo vệ răng vì lớp Ca5(PO4)3F
A.có thể phản ứng với H+ còn lại trong khoang miệng sau khi ăn.
B.không bị môi trường axit trong miệng sau khi ăn bào mòn.
C.là hợp chất trơ, bám chặt và bao phủ hết bề mặt của răng.
D.có màu trắng sáng, tạo vẻ đẹp cho răng.
Câu 4. Dãy nguyên tố nào dưới đây được xếp theo chiều tính oxi hóa tăng dần?
A. I < Br < Cl < F.
B. Br < I < Cl < F.
C.Cl < I < Br < F.
D.F < I < Br < Cl.
Câu 5. Đổ dung dịch AgNO3 vào dung dịch muối nào sau đây sẽ có kết tủa màu trắng xuất hiện?
A. NaF. B. NaCl.
C.NaBr. D.NaI.
Câu 6. Nguyên nhân chủ yếu làm cho đơn chất clo có tính oxi hóa mạng hơn đơn chất nitơ ở điều kiện thường là
A.clo có độ âm điện mạnh hơn oxi.
B.clo không tồn tại trong tự nhiên còn nitơ lại rất phổ biến.
C.nguyên tử clo có nhiều electron hơn nguyên tử nitơ.
D.liên kết trong phân tử clo là liên kết đơn còn trong phân tử nitơ là liên kết ba.
Câu 7. “Chảo chống dính” cõ lẽ là vật dụng không thể thiếu với các bà nội trợ hiện nay bởi những công dụng tuyệt vời của nó như: chiên thức ăn không bị dính, tiết kiệm dầu ăn... Sở dĩ, “không dính” vì mặt trong của chảo được tráng một lớp polime nhiệt dẻo có tính bền cao với các dung môi và hóa chất. Hợp chất được nhắc tới trong trường hợp này là
A. (-CF2-CF2-)n. B. (-CBr2-CBr2-)n.
C.(-CCl2-CCl2-)n. D. (-CI2-CI2-)n.
Câu 8. Đặc điểm chung của các nguyên tố nhóm halogen là
A. ở điều kiện thường là chất khí.
B. là chất oxi hóa mạnh.
C. tác dụng mạnh với H2O.
D. vừa có tính oxi hóa vừa có tính khử.
Câu 9. Đầu thế kỷ 19 người ta sản xuất natri sunfat bằng cách cho axit sunfuric đặc tác dụng với muối ăn. Khi đó, xung quanh các nhà máy sản xuất bằng cách này, dụng cụ của thợ thủ công rất nhanh hỏng và cây cối bị chết rất nhiều. Người ta đã cố gắng cho thoát khí thải thoát ra bằng những ống khói cao tới 300m nhưng tác hại của khí thải vẫn tiếp diễn, đặc biệt là khí hậu ẩm. Hãy chó biết khí thải đó có chứa thành phần chủ yêu nào trong các chất sau?
A.HCl. B.SO2.
C.H2SO4. D.Cl2.
Câu 10. Cho 500 ml dung dịch NaOH 1,8 M phản ứng với 500 ml dung dịch FeCl3 0,8 M thu được dung dịch A và chất rắn B. khối lượng chất rắn B là
A.3,21 g. B.21,4 g.
C.32,1 g. D.16,05 g.
Câu 11. Clorua vôi là hỗn hợp của
A.CaOCl, H2O. B.Ca(OCl)2, H2O.
C.CaOCl2, H2O. D.CaCl2, CaOCl, H2O.
Câu 12. Clo vừa là chất oxi hóa vừa là chất khử trong phản ứng của clo với
A.hiđro.
B.sắt.
C.dung dịch NaBr.
D.dung dịch NaOH.
Câu 13. Cho dung dịch sắt (II) clorua, thêm dư vào dung dịch axit clohiđric, sau đó thêm 0,5 gam một hỗn hợp muối kali clorua và kali nitrat. Sau phản ứng thu được 100 ml một chất khí (ở đktc và đã được làm khô). Thành phần phần trăm về khối lượng của hỗn hợp muối kali chorua và kali nitrat lần lượt là
A.18,90%; 81,1%.
B.9,82%; 90,18%.
C.90,18%; 9,82%.
D.29,46%; 70,54%.
Câu 14. Brom bị lẫn tạp chất là clo, để thu được brom cần làm cách nào sau đây?
A.Dẫn hỗn hợp đi qua dung dịch H2SO4 loãng.
B.Dẫn hỗn hợp đi qua nước.
C.Dẫn hỗn hợp đi qua dung dịch NaBr.
D.Dẫn hỗn hợp đi qua dung dịch NaI.
Câu 15. Cho hình vẽ sau
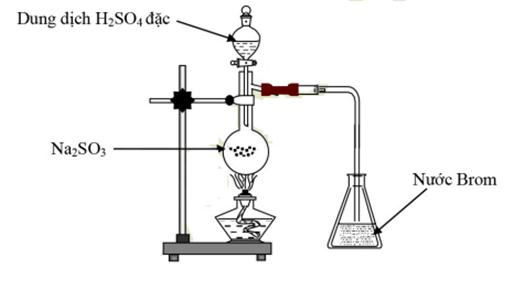
Hiện tượng xảy ra trong bình eclen chứa brom là
A.có kết tủa xuất hiện.
B.dung dịch brom bị mất màu.
C.vừa có kết tủa, vừa mất màu dung dịch brom.
D.không co phản ứng xảy ra.
Câu 16. Có các hóa chất: K2Cr2O7, HCl, KMnO4, MnO2, NaCl, HClO, H2SO4, KClO3. Những chất được sử dụng để điều chế Cl2 trong phòng thí nghiệm là
A.K2Cr2O7, HCl, KMnO4, MnO2, NaCl, HclO.
B.K2Cr2O7, HCl, KMnO4, MnO2, KClO3.
C.K2Cr2O7, HCl, KMnO4, MnO2, H2SO4.
D.K2Cr2O7, HCl, KMnO4, MnO2, NaCl, HClO, H2SO4.
Câu 17. Để điều chế được 16,25 gam FeCl3 cần cho sắt phản ứng vừa đủ với V lít khi clo (đktc). Giá trị của V là
A.2,24 lít. B.22,4 lít.
C.6,72 lít. D.3.36 lít.
Câu 18. Cho biết số hiệu nguyên tử của các nguyên tố N, F và P lần lượt là 7, 9 và 15. Dựa vào cấu hình electron và qui luật biến đổi tính chất của các nguyên tố trong bảng tuần hoàn, hãy so sánh tính phi kim của P và F.
A.F có tính phi kim mạnh hơn P
B.P có tính phi kim mạnh hơn F.
C.F có tính phi kim bằng P.
D.không so sánh được.
Câu 19. Nhận định nào sau đây sai khi nói về flo?
A. Là phi kim hoạt động mạnh nhất.
B. Có nhiều đồng vị trong tự nhiên.
C. Là chất oxi hóa rất mạnh.
D. Có độ âm điện lớn nhất.
Câu 20. Cho hỗn hợp gồm các chất sau: Mg(HCO3), CuO, Ag, CuS, KOH, KNO3, Fe(OH)3, Na2SO4. Số chất có khả năng tác dụng với dung dịch HCl là
A.3. B.4.
C.5. C.6.
Câu 21. Để nhận biết 5 lọ mất nhãn đựng các dung dịch: HCl, KOH, Ca(NO3)2, BaCl2, thuốc thử cần dùng là
A.quỳ tím và dung dịch AgNO3.
B.dung dịch AgNO3.
C.quỳ tím và dung dịch H2SO4.
D.quỳ tím.
Câu 22. Hòa tan 31,6 gam KMnO4 bằng một lượng vừa đủ 400 ml dung dịch HCl thu được V lít khí (đktc). Giá trị của V là
A.1,12 lít. B.11,2 lít.
C.22,4 lít. D.2,24 lít.
Câu 23. Cho các phát biểu sau
(a) Đổ dung dịch AgNO3 vào dung dịch NaF thu được kết tủa.
(b) Người ta dùng lọ thủy tinh để đựng dung dịch axit flohiđric.
(c) Clorua vôi là muối tạo bởi một kim loại liên kết với hai loại gốc axit.
(d) Tính oxi hóa của các đơn chất halogen giảm theo thứ tự I2, Br2, Cl2, F2.
Phát biểu đúng là
A.(b). B.(c).
C.(a). D.(d).
Câu 24. Phát biểu nào sau đây không đúng?
A. Axit flohiđric là một axit yếu, có tính chất ăn mòn thủy tinh.
B. Các nguyên tố halogen đều tồn tại ở trạng thái khí và phân tử chỉ gồm một nguyên tử.
C. Flo oxi hóa nước dễ dàng ở nhiệt độ thường nên không thể tạo được nước flo.
D. Khi điện phân dung dịch muối ăn không có màng ngăn, ta thu được nước Javen.
Câu 25. Trong phản ứng hóa học sau:
\(S{O_2} + B{r_2} + 2{H_2}O \to {H_2}S{O_4} + 2HBr\).
Vai trò của Br2 là
A.chất khử
B.chất bị khử.
C.chất bị oxi hóa.
D.chất khử và chất oxi hóa.
Câu 26. Để điều chế clo trong công nghiệp ta phải dùng điện phân có màng ngăn cách hai điện cực để
A.khí Cl2 không tiếp xúc với dung dịch NaOH.
B.thu được dung dịch nước Javen.
C. bảo vệ các điện cực không bị ăn mòn.
D.Cả A, B. C đều đúng.
Câu 27. Cho phương trình:
\({K_2}C{r_2}{O_7} + HCl \to CrC{l_3} + C{l_2} + KCl + {H_2}O\)
Tỉ lệ giữa số phân tử HCl đóng vai trò là chất khử và số phân tử HCl tham gia phản ứng
A. 1: 2. B. 1: 14.
C. 3: 14. D. 3: 7.
Câu 28. Cho dung dịch chứa 6,03 gam hỗn hợp gồm hai muối NaX và NaY ( X, Y là hai nguyên tố có trong tự nhiên, ở hai chu kì liên tiếp thuộc nhóm VIIA, số hiệu nguyên tử ZX < ZY) vào dung dịch AgNO3 (dư), thu được 8,61 gam kết tủa. Phần trăm khối lượng của NaX trong hỗn hợp ban đầu là
A.58,2%. B.41,8%.
C.52,8%. D.47,2%.
Câu 29. Dung dịch HCl không tác dụng với cặp chất nào sau đây?
A.Mg, Na. B. Na2SO4, Ag.
C.Na2CO3, SO2. D.NH3, Fe.
Câu 30. Hòa tan khí clo vào dung dịch KOH đặc nóng, dư thu được dung dịch chứa các chất thuộc dãy nào sau đây?
A.KCl, KClO.
B.KCl, KClO3.
C.KCl, KOH.
D. KCl, KClO3, KOH.
