Bài 32: Hiđro sunfua - lưu huỳnh đioxit - lưu huỳnh trioxit
Bài Tập và lời giải
Câu 32.1.
Cho phản ứng : \(SO_2 + 2H_2S → 3S + 2H_2O\)
Phát biểu nào sau đây đúng?
A. Lưu huỳnh bị oxi hoá và hiđro bị khử.
B. Lưu huỳnh bị khử và không có chất nào bị oxi hoá
C. Lưu huỳnh bị khử và hiđro bị oxi hoá
D. Lưu huỳnh trong \(SO_2\) bị khử, lưu huỳnh trong \(H_2S\) bị oxi hoá.
Chất nào sau đây vừa có tính oxi hóa, vừa có tính khử?
A. H2SO4 B.H2S C. SO2 D. SO3
Đề bài
Khí CO2 có lẫn tạp chất là SO2. Để loại bỏ tạp chất ta sục hỗn hợp vào dung dịch nào sau đây?
A.Dung dịch Br2 dư
B. Dung dịch Ba(OH)2 dư
C. Dung dịch Ca(OH)2 dư
D. Dung dịch NaOH dư
Đề bài
Cho sơ đồ phản ứng:
\({H_2}S + KMn{O_4} + {H_2}S{O_4}\xrightarrow{{}}{H_2}O + S + MnS{O_4} + {K_2}S{O_4}\)
Hệ số của các chất tham gia phản ứng là dãy số nào sau đây?
A. 3, 3, 5 B. 5, 2, 3
C. 2, 2, 5. D. 5, 2, 4
Đề bài
Ba thí nghiệm được tiến hành với những khối lượng Zn bằng nhau và với \(50 cm^3\) dung dịch loãng \(H_2SO_4\) 2M. PTHH của phản ứng :
\(Zn + H_2SO_4 → ZnSO_4 + H_2↑\)
Bảng dưới đây cho biết các điều kiện của mỗi thí nghiệm :
|
Thí nghiệm |
Kẽm |
Nhiệt độ (°C) |
|
1 |
bột |
30 |
|
2 |
lá |
20 |
|
3 |
lá |
30 |
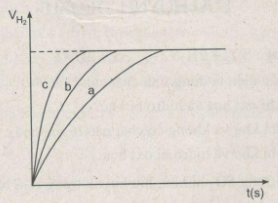
Khí hiđro thu được trong mỗi thí nghiệm được ghi lại theo những khoảng cách nhất định về thời gian cho đến khi phản ứng kết thúc, được biểu diễn bằng đồ thị sau :
a) Rút ra được những nhận xét gì khi so sánh hiện tượng phản ứng của :
- Thí nghiệm 1 và thí nghiệm 3 ?
- Thí nghiệm 2 và thí nghiệm 3 ?
b) Hãy quan sát đồ thị trên để cho biết các đường cong a, b, c biểu thị cho những thí nghiệm nào ?
c) Ghi thể tích khí \(H_2\) trên trục y khi phản ứng kết thúc. Biết rằng ở điều kiện phòng thí nghiệm, 1 mol khí có thể tích là 24 lít và Zn còn dư sau các thí nghiệm.
Đề bài
Trong phòng thí nghiêm, bạn em khảo sát thí nghiệm dùng dung dịch HCl dư tác dụng với một khối lượng nhỏ FeS. Cứ sau một khoảng cách thời gian là 20 giây, bạn em lại ghi thể tích khí thoát ra. Kết quả ghi được như sau (xem bảng) :
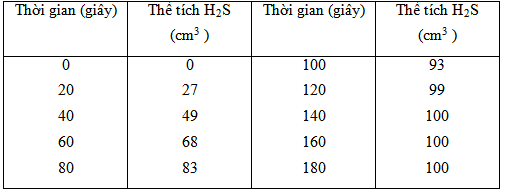
a) Viết PTHH của phản ứng.
b)Vẽ đồ thị biểu diễn thể tích khí \(H_2S\) thu được (trên trục tung) theo thời gian (trên trục hoành).
c) Hãy dùng đồ thị để tìm :
- Thể tích khí \(H_2S\) thu được ở thời điểm 50 giây.
- Khoảng cách thời gian nào thì phản ứng xảy ra nhanh nhất ? chậm nhất ?
- Thời gian là bao nhiêu giây kể từ khi phản ứng xảy ra cho đến khi phản ứng kết thúc ?
d) Em hãy phác hoạ trên đồ thị này một đồ thị biểu diễn thể tích khí \(H_2S\) thu được, nếu bạn em thay bằng dung dịch HCl khác có cùng thể tích nhưng có nồng độ cao hơn.
Đề bài
Từ những chất sau : \(Cu, S, H_2S, O_2, Na_2SO_3, H_2SO_4\) đặc và dung dịch \(H_2SO_4\) loãng, hãy viết PTHH của phản ứng điều chế \(SO_2\).
Đề bài
Đốt cháy hoàn toàn 3,4 gam hợp chất A, thu được 2,24 lít khí \(SO_2\) (đktc) và 1,8 gam \(H_2O\).
a)Hãy xác định công thức phân tử của hợp chất A.
b) Viết PTHH biểu diễn phản ứng cháy của hợp chất A.
c)Dẫn khí \(SO_2\) thu được ở trên vào 146,6 gam dung dịch, trong đó có hoà tan 0,3 mol NaOH. Hãy xác định nồng độ phần trăm các chất có trong dung dịch sau phản ứng.
Đề bài
a) Tại sao dung dịch \(H_2S\) trong nước để lâu ngày trở nên vẩn đục?
b)Hãy giải thích vì sao trong tự nhiên có nhiều nguồn phóng thải ra khí \(H_2S\) (núi lửa, xác động vật bị phân huỷ) nhưng lại không có sự tích tụ khí đó trong không khí?
c) Hãy giải thích vì sao các đồ vật bằng bạc để lâu ngày thường bị xám đen?
d) Tại sao người ta có thể nhận biết khí \(H_2S\) bằng tờ giấy tẩm dung dịch \(Pb(NO_3)_2\)?
Đề bài
Trong phản ứng hoá học, các chất : \(S, H_2S, SO_2, H_2SO_3 \)có thể đóng vai trò chất oxi hoá hay chất khử ? Hãy viết PTHH của phản ứng để minh hoạ cho mỗi trường hợp.
Đề bài
Cho m gam hỗn hợp hai muối \(Na_2CO_3\) và \(NaHSO_3\) có số mol bằng nhau tác dụng với dung dịch \(H_2SO_4\) loãng, dư. Khí sinh ra được dẫn vào dung dịch \(Ba(OH)_2\) dư thu được 41,4 gam kết tủa. Xác định m.
Đề bài
Dẫn từ từ 28 gam hỗn hợp X gồm (\(CO_2, SO_2\)), (\(d_{X/O_2}\) = 1,75) qua 500 ml dung dịch hỗn hợp (NaOH 0,7M ; \(Ba(OH)_2\) 0,4M) được m gam kết tủa. Xác định m.